リチウムイオン電池の次を狙うは、リチウム空気電池(2)
2009年11月26日
空気中の酸素を使う「空気電池」とは?
──空気電池とは、いったいどういうものなのでしょう?
正極活物質として、空気中の酸素を使うということです。空気電池は、人間の呼吸と同じように、酸素を取り入れてエネルギーを生み出します。
従来の電池は、負極と正極の活物質を合わせた重量でエネルギー密度を計算していました。空気電池なら、正極活物質は空気ですから、重量はほとんど負極活物質だけになり、圧倒的にエネルギー密度が高くなります。
空気電池はさまざまな金属で研究されていますが、最も実用化が進んでいるのは亜鉛です。亜鉛空気電池(一次電池)は補聴器などに用いられています。
リチウム空気電池は、空気電池の中ではいちばん歴史が浅いでしょうね。最初のリチウム空気電池は、1996年に米国の研究グループが開発しました。ただ、最初のリチウム空気電池は、「リチウム酸素電池」と言うべきではないかと私は思います。なぜかというと、水分を除いた酸素をボンベに詰め、それを負極活物質として使っていたからです。空気中の水分が電池内の電解液に溶け込み負極側に行ってしまうと、水素が発生してしまいますから、これを避けるために酸素ボンベを使用したのです。
また、このリチウム酸素電池には、もう一つ大きな欠点がありました。電解液中のリチウムイオンと酸素が反応することで、酸化リチウムが生じるわけですが、酸化リチウムは固体で水に溶けません。
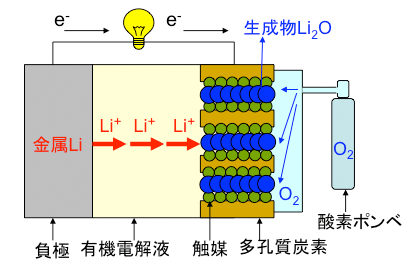
従来のリチウム空気電池では、酸化リチウムが生成されてしまっていた。酸化リチウムが触媒の表面をコーティングするとそれ以上、反応が進まなくなってしまう。(独立行政法人産業技術総合研究所(AIST)提供)
──酸化リチウムが生じると、どのような問題があるのでしょう?
電極の表面が酸化リチウムでコーティングされてしまって、それ以上酸素を取り入れることができず、反応が進まなくなるのです。あるところまで来ると、いきなり放電が止まっていました。
この「リチウム酸素電池」でもリチウムイオン電池よりはエネルギー密度は高いわけですが、これでは空気電池のメリットを生かし切れていません。
ならば、酸化リチウムのような固体が生じない反応を使えば、放電をずっと長く続けられるのではないか。私たちはそう考えました。
従来のリチウム空気電池が持っていた欠点が解決された
──どういう反応を利用したのですか?
私たちが開発したリチウム空気電池では、負極の金属リチウムがリチウムイオン(Li⁺)として電解液に溶け出します。一方、正極では、空気中の酸素と水が反応して、水酸化イオン(OH⁻)が生じます。
水酸化イオンとリチウムイオンが出会って生成されるのは、水酸化リチウム(LiOH)で、これは水に溶けるため電極の目詰まりが起こりません。
電解液はアルカリ性ですから、触媒として高価な白金ではなく、安価な金属酸化物、例えば酸化マンガンなどを使うことができます。
山路達也の「エコ技術研究者に訊く」
過去の記事
- 超低消費電力を実現できるか? 「板バネ」ナノマシンコンピュータ(3)2011年3月24日
- 超低消費電力を実現できるか? 「板バネ」ナノマシンコンピュータ(2)2011年3月24日
- 超低消費電力を実現できるか? 「板バネ」ナノマシンコンピュータ(1)2011年3月24日
- オーランチオキトリウムが、日本を産油国にする(4)2011年2月25日
- オーランチオキトリウムが、日本を産油国にする(3)2011年2月25日

